都是靶向Aβ的药物
大家都躺在阿尔兹海默的III期坟墓
为什么aducanumab爬起来独秀?
(暂且认为Biogen的EMERGE三期成功了)
友提:文末有福利

上一篇方姨详细地分析了Biogen的aducanumab实现神奇逆转的两项III期临床试验数据结果,可以说这一次的大翻盘靠的是统计师立功了。(原文链接:统计师立功了?首个阿尔茨海默药物要上市了?)
实际上关于这个大瓜,这两天大家看到的文章也很多。但很多文章仅限于传递这个消息,就像某些大厂的公号文章都阅读上十万了,好像也没看到有人解读或者反问下,为什么是aducanumab?
大家都是靶向β-淀粉样蛋白(β-amyloid,Aβ)的单克隆抗体药物,为何aducanumab没有掉入III期黑洞,既实现清除β-淀粉样蛋白,也达到了认知功能改善的终点呢?
中国人现在就信奉一句话,打铁还需自身硬。如果没有内在深层次的原因,就算统计师们玩出花儿来,也无力回天啊。
下面方姨就假装比较专业、尝试做一下反思和回顾,希望抛砖引玉,整理下对这类研发公司的投资思路。

01
β-淀粉样蛋白级联反应假说
回顾一下阿尔兹海默症的研究,搞了这么多年,大家还是倾向于认为Aβ是导致阿尔茨海默症的原因,通过对这个蛋白的不断观察和研究,形成一套淀粉样蛋白级联反应假说。
这个假说的基本观点为Aβ的沉积是发病的始发因素,Aβ的聚集具有神经毒性。
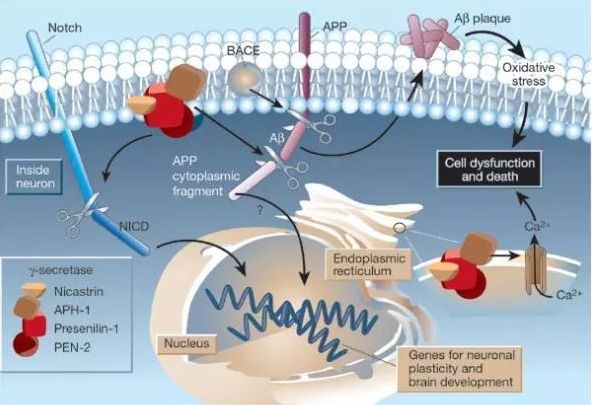
Aβ产生的增加和聚集,尤其是Aβ42 在脑组织沉积会导致形成老年斑。Aβ42 的沉积能引起神经元内Ca离子浓度增加,激活蛋白激酶的活化,引起微管相关的tau蛋白高度磷酸化,使螺旋丝受损,继而形成纤维缠结。
Aβ的沉积还能引起各种免疫炎症反应和神经毒性级联反应,引起广泛的神经元变性,甚至死亡,主要在海马和大脑皮层,出现渐进性的神经递质减少,主要是胆碱能和多巴胺能递质,最终导致记忆和认知功能障碍。
Aβ产生细胞损失甚至死亡的具体机制为(1)引起细胞内钙超载,使细胞内环境失衡;(2)促进活性氧自由基产生,产生氧化损伤;(3)激发的免疫反应,主要是小胶质细胞和星形胶质细胞的激活释放细胞因子,产生细胞毒作用。
02
清除Aβ是否就意味着成功了?
上面这一套搞得很有逻辑之后,业内这些大拿们的反应都是,OK,现在大家知(cai)道(de)是这个蛋白的事,无非就是搞定这个蛋白,要么抑制阻断你的合成,要么主动结合废掉你的功能。
那么这一套东西业界大拿们都很拿手啊,上啊,干就完了,又不是没那条件。。。

结果几十年来,专门设计用于清除大脑中的Aβ的药物不少,然而这一类的药物每次在这个领域失败了。
大家可以用你们的小手轻轻的搜一下clinicaltrials.gov,只看III期,倒在I期、II期的我们就不再盘了。出来的结果,业界发起的针对Aβ治疗AD的III期临床试验有45个。。。。
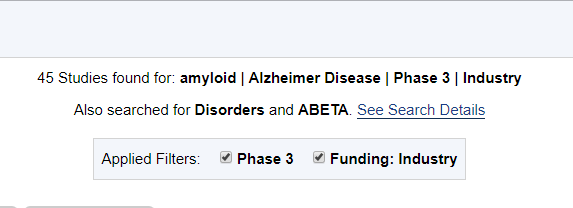
浏览一圈,几乎都是失败,或者没有结果也不知道什么状态。
而且还有的药物在清除Aβ的效果上非常好,但还是无法改善认知功能持续恶化、或者无法表现的比安慰剂强点。
换句话说,在认知功能这个终点上,统计学上,大家都是失败了。。。
所以这么些年来,前仆后继的失败造就了阿尔兹海默症III期黑洞的美誉。

这么多失败,让大家对Aβ和阿尔兹海默症的相关性都发出了疑问,我们是不是把相关和因果搞错了?这是医学领域最常见的错误。
到底是Aβ增多导致认知功能下降,还是认知功能下降使得Aβ增多呢?是不是Aβ增多只是阿尔兹海默病的一种症状?是疾病导致的代谢产物而非致病原因本身?毕竟我们根本不知道它到底是为什么会大量出现在我们脑壳儿里的。
03
那些倒下的靶向Aβ的药物
今年7月,诺华、安进和班纳阿尔茨海默氏症研究所决定停止对BACE1抑制剂CNP520(umibecestat)的研究。该决定是因为患者在治疗期间症状持续恶化,并且参与研究的潜在益处未超过风险。
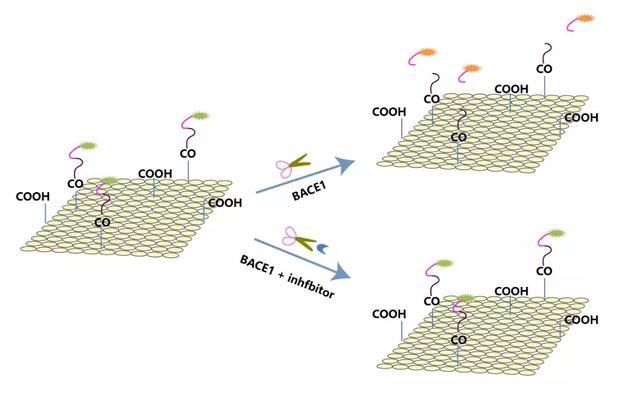
CNP520是BACE1抑制剂,BACE1分子就像一把剪刀,可以切割神经元膜蛋白,产生淀粉样蛋白片段,其中一些可能会导致阿尔兹海默症。
另一个由默沙东开发的BACE1抑制剂verubecestat,2017年的时候也是同样的厄运,当时分析完II期临床数据,就决定暂停其III期临床。实际上,数据显示verubecestat能够将Aβ生成量减少高达90%之多。
今年1月,罗氏宣布终止crenezumab 治疗早期阿尔茨海默病患者(前驱或轻度AD患者)的两项III期CREAD I和CREAD 2临床研究。
不过在2018年,罗氏宣布重启推动 gantenerumab 的两项大型 III期临床试验GRADUATE-1 和 GRADUATE-2。三年前 gantenerumab的失败还历历在目,在这一次重启前,罗氏与合作伙伴 MorphoSys 一直在进行安全性研究,为确保更高的暴露剂量不会引起难以控制的副作用,尤其是 ARIA-E(一种大脑水肿的形式),这一次gantenerumab应用了新的抗体产生技术。希望在改善安全性后,通过提高剂量来获得更好的结果。
失败者的名单还很长,什么礼来的semagacestat、solanezumab以及lanabecestat,辉瑞与强生的bapineuzumab,强生自己的atabecestat。
不禁让人陷入沉思,想起相对论里面的一条著名定义。。。

04
能不能期待别的Aβ和aducanumab一样逆转?
好了,现在aducanumab提高剂量,重新搞搞统计成功了,上面那些已经宣告死亡的呢?是不是可能再次翻盘?说不定分析分析,压中一个,也来一个一夜暴涨40%?
希望可能是很渺茫的。原因就在于这些不同的药物的发现或开发过程是完全不一样的,大部分的研究人员,都是传统的点对点的研发思路,既然大家假设Aβ这个理论正确,那就真对Aβ这个靶点各显神通。
比如上面那一堆stat结尾的分子,针对BACE1这个机制;上面那一堆mab的单抗,都是通过噬菌体展示技术合成不同的抗体,通过不同的功能或方式,来降解β-淀粉样蛋白。
但是aducanumab不太一样,它不同于上述那些单抗合成选择的过程,并不是通过噬菌体展示技术判断是否能达到清除β-淀粉样蛋白筛选出来的。
它是Neurimmune公司从两组不同的细胞库结合分析出来的。一组库是健康老年人的B细胞库,这些老年人虽然年事已高,但是没有表现出认知能力方面的下降,或者认知能力下降的速度要比普通人缓慢得多;另一组库是已经出现了认知能力损害的老年人,但这些老年人相对其他出现认知能力损害的老年人,其认知能力下降速度异乎寻常的慢。
所以开发人员并不是从搞定Aβ的角度出发,而是猜测他们身体里可能有什么因素能够抵抗阿尔茨海默症的进展。然后他们从这两组细胞库中寻找细微的差异,而aducanumab就这样诞生了。
aducanumab的发现有点像逆向工程。开发人员并没有按照一项特定的任务或目标来设计答案,而是采用了一种方法,即答案已经存在,只需定位即可。
在不太复杂的疾病机制下,这样的逆向工程是比较好理解并执行的。但是我们并不清楚阿尔茨海默症的机制,而大脑也是迄今为止最复杂的器官。所以最初Biogen从Neruimmune那获得aducanumab的时候,成功的可能性也是微乎其微的。
所以反过来看,aducanumab能清除Aβ,更像是一个副作用。其对减缓或阻碍认知能力下降的作用机制还是未知的,就像阿尔茨海默症的发病机制一样,尚不清楚。
05
最后转一个好友的评论:
现在很多公司出来讲,我也有PD-1/L1,我也做BTK,我管线里也有PRAP,我还有EGFR/EGFR-TKI。你是人源单抗是吧,那我纳米单抗,骆源单抗,双抗。你有car-T,那我car-B, car-N,car-K。反正什么热我有什么。照着这样的赛道投下去,怕都是要血本无归。
所以,还是要看看这些东西是怎么搞出来的,研发思路是什么,研发资料数据什么的还是要梳理,毕竟打铁还需自身硬,不忘初心,方得始终。
文末福利,关注公众号,并留言“阿尔茨海默”,直接获取IQVIA的【攻破阿尔茨海默症的五大难题A CALL TO ACTION: ALZHEIMER'S DISEASE ON THE THRESHOLD OF CHANGE】。

往期回顾
统计师立功了?首个阿尔茨海默药物要上市了?
15亿美元!豪森豪赌人工智能药物发现
艾伯维58亿美金Rova-T宣布洗白
枯木逢春?最难成药的老靶点传来好消息
要命还是要钱?打一针212.5万美元的救命药获批
首个基于甲胎蛋白标记物的抗肝癌药物获批

“看我的眼神
你怎么舍得
就这样狠心离开”

扫描二维码
关注微信号

(特别声明:上述图片及素材来自网络,如有侵权,立即删除)
喜欢本篇内容请给我们点个在看
